如今,益生菌备受青睐。从巧克力到泡菜,从护手霜到婴幼儿配方奶粉,越来越多的人在购买益生菌产品或补充剂来改善自身健康。但是新研究表明,益生菌可能并不像我们想得那样有效。研究人员通过对人体肠道一系列的实验表明,很多人的肠道会阻止普通益生菌成功定植。此外,服用益生菌来抵消抗生素的影响会延缓肠道细菌和肠道基因表达恢复到正常状态。这项研究分为两篇论文发表在9月6日的《Cell》上。


研究通讯作者,以色列魏茨曼科学研究所的免疫学家Eran Elinav说:“益生菌的益生作用已经得到了很多支持,尽管据我所知很多文献是有争议的。因此,我们想要证实,市面上销售的益生菌是否能像预期的那样在胃肠道中定居,以及这些益生菌是否会对人类宿主产生影响。令人惊讶的是,我们发现很多健康志愿者对益生菌都表现出抗性,益生菌无法在他们的肠道中定植。这表明,益生菌不应该被认为是一种普遍适用的补充剂。相反,它们应该根据个体的实际情况来使用。”
虽然过去也有研究关注过类似问题,但他们都将患者的排泄物用作肠道微生物活动的代表。相反,Elinav和同事Eran Segal(魏茨曼科学研究所的计算生物学家)的研究团队与特拉维夫医学中心的胃肠病学负责人Zamir Halpern合作,直接对肠道中的细菌生存情况进行测试。
在第一项研究中,有25名健康志愿者接受了上消化道内镜检查和结肠镜检查,以对肠道中的基线微生物组进行采样。其中15名志愿者再被分为两组。第一组服用常见的益生菌菌株,第二组服用安慰剂。之后这两组都再次接受上消化道内视镜检查和结肠镜检查以评估其内部反应,然后再进行两个月的随访。
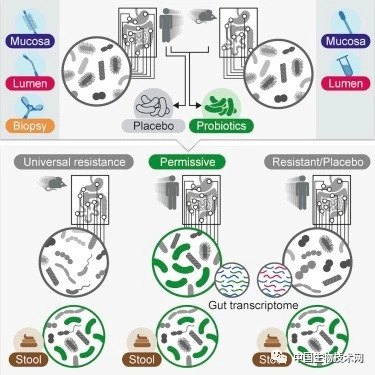
图片来源:《Cell》
科学家们发现,益生菌能够在一些人的胃肠道中成功存活下来,他们被称为“持留者”,而另外一些称为“抵抗者”的肠道微生物组则会驱逐益生菌。此外,“持留者”和“抵抗者”模式可以决定益生菌是否能够影响给定人的原生微生物组以及基因表达。研究人员可以通过检测他们的基线微生物组和肠道基因表达谱来预测一个人是否会成为“持留者”或“抵抗者”。
他们还发现,粪便与人体内的微生物组功能只存在部分相关性,因此以往依赖于粪便的研究可能会出现误导。
Segal说:“尽管益生菌出现在了所有服用益生菌的志愿者的粪便中,但是它们却只存在于部分志愿者的肠道中,而在肠道中存活下来才是服用益生菌的初衷。如果只有部分人能够接受益生菌,而其他人是排斥益生菌的,那么我们所服用的常见益生菌的益生作用可能并不像我们认为的那样普遍适用。这表明了肠道微生物组在导致个体临床差异方面的重要作用。”
在第二项研究中,研究人员对患者是否应该服用益生菌来抵消抗生素的影响提出了质疑,因为患者们通常被告知要这么做是为了恢复抗生素治疗之后的肠道微生物群。为了研究这点,21名志愿者接受了抗生素疗程,然后被随机分到三个组中。第一组是“观察和等待”组,让他们的微生物组自行恢复。第二组服用第一项实验中使用的相同益生菌。第三接则用自体粪便微生物组移植物(aFMT)治疗,该移植由他们自己的细菌组成,这些细菌在给予抗生素之前已被收集。
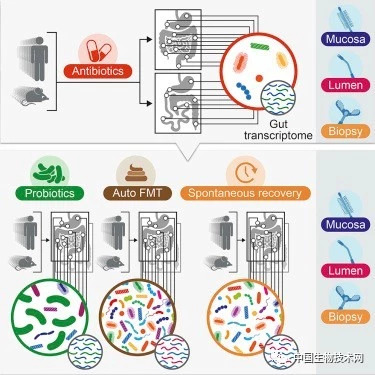
图片来源:《Cell》
在抗生素被清理干净之后,普通益生菌能够很容易地在第二组中的所有参与者的肠道中存活,但是令研究团队意外的是,益生菌的定植会在接下来的几个月中阻止宿主的正常微生物组和肠道基因表达恢复到正常状态。相比之下,接受aFMT治疗的第三组的天然肠道微生物组和基因表达在几天内就恢复到了正常状态。
Elinav说:“当前的普遍认为益生菌是无害且对所有人都有益。而这些结果表明,服用抗生素之后使用益生菌会带来潜在的副作用,甚至可能带来长期后果。相比之下,使用自己的微生物来恢复肠道是一种个性化的纯自然疗法,能够完全消除抗生素的影响。”
Segal补充说:“这项研究带来了新的诊断方法,将使我们从服用益生菌的普遍经验中获益,现在我们可以根据个体特征来为不同的人提供定制化的治疗方法。”
参考文献:
1、Post-Antibiotic Gut Mucosal Microbiome Reconstitution Is Impaired by Probiotics and Improved by Autologous FMT
DOI:https://doi.org/10.1016/j.cell.2018.08.047
2、Personalized Gut Mucosal Colonization Resistance to Empiric Probiotics Is Associated with Unique Host and Microbiome Features
DOI:https://doi.org/10.1016/j.cell.2018.08.041
转自中国生物技术网